Спонтанный перелом новорожденных
У детей относительно упругие кости, плотная эластичная надкостница и хорошо развитые мягкие ткани, защищающие от переломов. Тем не менее уже в первые десять лет жизни каждый 15 россиянин перенес перелом [1] . К пятнадцати годам хоть раз в жизни носил гипс (или перенес операцию по поводу перелома) уже каждый восьмой ребенок. Чаще всего дети ломают кости предплечья – 37,4% всех переломов. Чуть реже повреждаются кости голени и лодыжки (22%), на третьем месте по частоте – переломы ключицы (9%).
Чем отличаются детские переломы от взрослых, возможные последствия травмы и современные методы восстановления – в нашем обзоре.
Особенности переломов костей у детей
Кости у детей содержат больше воды, органических веществ и меньше минеральных солей, чем у взрослых. Между эпифизами – «головками» трубчатой кости, где она сочленяется с суставом, – и диафизами – «трубками» кости с костномозговым каналом – у детей находятся хрящевые зоны роста. В этих зонах активно делятся клетки, обеспечивая постоянное удлинение костей. И это самый слабый участок детских костей. Увеличение костей в поперечнике происходит за счет костеобразования со стороны надкостницы, более толстой и эластичной. Эти особенности приводят к тому, что у детей появляются особые виды переломов, практически не встречающиеся у взрослых:
- надлом или перелом по типу «зеленой ветки» – перелом не «завершается», на противоположной участку перелома стороне кости надкостница остается целой;
- поднадкостничный перелом – сломанная кость остается покрытой неповрежденной надкостницей;
- эпифизиолизы, остеоэпифизиолизы, метаэпифизиолизы – разрывы по линии хряща зоны роста (механизм этой травмы соответствует механизму вывиха у взрослых, и клиническая картина часто похожа) с отрывом эпифиза от метафиза (губчатого вещества между эпифизом и диафизом) или с частью метафиза (зависит от анатомического строения конкретной кости);
- апофизиолизы – отрыв по ростковой зоне внесуставного «выступа» кости – апофиза, к которому крепятся мышцы.
В то же время у детей крайне активный обмен веществ, а значит, костная ткань обновляется быстрее, чем у взрослых. Поэтому и переломы срастаются быстрее, а образование ложного сустава или дефекта костей у ребенка скорее казуистика. Из-за активного роста у детей самопроизвольно устраняется смещение костных отломков, в связи с чем репозицию (совмещение костей) при переломах со смещением в детском возрасте обычно проводят без операции.
Виды и последствия переломов у детей
По типу воздействия переломы бывают травматические и патологические . Патологические переломы появляются, когда кость изначально ослаблена из-за нарушенной структуры (например, синдром несовершенного остеогенеза или «хрустального человека») или опухолей, кист, остеомиелита. Патологические переломы у детей случаются редко.
По характеру повреждений окружающих тканей переломы могут быть закрытые и открытые , когда острые концы костей «прорывают» мягкие ткани. Открытые переломы у детей – чаще всего следствие тяжелой сочетанной травмы (например, в результате автомобильной аварии), они требуют обязательного хирургического вмешательства.
По соотношению костных отломков переломы могут быть без смещения , когда отломки сохраняют нормальное анатомическое соотношение, и со смещением , когда они сдвигаются относительно друг друга. У детей переломы без смещения, как правило, имеют смазанную клиническую картину и их трудно диагностировать. Возможен ошибочный диагноз ушиба, и, как следствие, из-за неправильного лечения конечность может искривиться, а ее функция – нарушиться.
Переломы со смещением проявляются «ярче», оставляя меньше возможностей для диагностических ошибок. Из-за способности детских (особенно у пациентов до семи лет) костей самоустранять смещение в процессе роста допускается неточная репозиция (хирургическое сопоставление, или вправление, костных отломков) при переломах диафиза («тела» трубчатой кости). Но если смещение винтовое, исправить его нужно обязательно, такие изменения самостоятельно не корригируются (не исправляются). Тщательная репозиция необходима при внутрисуставных переломах, иначе функция сустава может нарушиться, вплоть до его полной неподвижности.
Повреждение зоны роста может вызывать ее преждевременное закрытие. Пораженная конечность будет расти тем медленнее, чем младше ребенок, и тем заметнее окажется отставание.
Особая группа переломов у детей – компрессионные переломы позвоночника , которые часто могут оставаться незамеченными. Они возникают при падении с относительно небольшой высоты (что вроде бы не дает повода для беспокойства) и плохо выявляются на рентгенограммах. Дело в том, что при компрессионном переломе позвонок приобретает клиновидную форму, и это единственный рентгенологический признак патологии. При этом у детей клиновидная форма позвонков – возрастная норма. Поэтому при подозрении на подобный перелом рекомендованы не просто рентгенограмма, но КТ или МРТ.
Этапы лечения переломов
Поскольку у детей симптомы перелома не так явно выражены, как у взрослых, до прихода врача (в случае сомнения) лучше действовать исходя из того, что перелом есть. Возможные признаки перелома :
- припухлость, отек, резкая локальная боль в зоне травмы, особенно при осевой нагрузке (давить не надо, можно легко постучать по пятке или основанию ладони);
- ограничение движений (пострадавший всеми силами «бережет» сломанную конечность);
- укорочение конечности;
- видимая деформация конечности (если голень согнута под углом, вопросов обычно не возникает);
- костный хруст при попытке движения.
До прихода врача нельзя:
- вправлять отломки при открытом переломе;
- пытаться вернуть конечности «правильную» форму;
- причинять дополнительную травму, снимая одежду (штанину или рукав нужно разрезать).
Пострадавшую конечность фиксируют шиной, под которую подкладывают мягкую ткань. Шина обязательно должна заходить за суставы выше и ниже области перелома.
Это важно!
В случае перелома или подозрения на перелом у детей конечность фиксируется «как есть», не надо пытаться что-то исправить – это задача врача. Крупные кости (бедро, голень) фиксируют двумя шинами по обе стороны конечности. Если перелом открытый, рану накрывают чистой марлевой салфеткой, которую по краям фиксируют пластырем.
После фиксации следует вызвать скорую, либо, если позволяет состояние ребенка, довезти его в дежурную травматологическую поликлинику. Можно дать ребенку парацетамол.
В медицинском учреждении сделают рентгенограмму. Иногда бывает, что по первой рентгенограмме точно диагностировать перелом не получается из-за возрастных особенностей. Тогда обязательна повторная ренгенография через семь-десять дней, когда из-за начавшейся консолидации (срастания) костей перелом на снимке станет заметнее. Поэтому, когда врач порекомендует сделать контрольный рентген через неделю, пренебрегать этой рекомендацией ни в коем случае не стоит.
Лечение переломов может быть консервативным и оперативным .
Методы лечения переломов у детей
94% переломов у детей требуют консервативного лечения [2] . Врач сопоставляет костные отломки и накладывает на конечность гипсовую лангету, неподвижно фиксируя область перелома и два смежных сустава. Кроме гипса могут быть использованы современные легкие материалы на основе пластика, благодаря которым можно принимать душ в период фиксации перелома. Продолжительность фиксации зависит от возраста ребенка и поврежденной кости и может составлять от 7 до 42 дней. Раз в неделю необходим рентгенологический контроль состояния костных отломков.
При переломах бедренной кости используют скелетное вытяжение, поскольку мышцы бедра слишком сильны и смещают отломки костей.
Операции для фиксации костных отломков у детей применяются редко. Показания к оперативному вмешательству следующие:
- внутри- и околосуставные переломы со смещением и ротацией костного фрагмента;
- при диафизарном переломе после двух-трех попыток репозиций сохраняется слишком сильное смещение отломков;
- открытые переломы;
- неправильно сросшиеся переломы с выраженной деформацией кости;
- патологические переломы;
- повреждение магистрального сосуда или нерва;
- межотломковая интерпозиция (между отломками костей оказываются мягкие ткани).
При операции чаще всего используют спицевой остеосинтез, т.е. соединение отломков костей посредством спиц, как максимально щадящий. Металлические пластины применяют у детей старшего возраста при скошенных и винтовых переломах диафизов крупных костей: бедренной, большой берцовой. При любом вмешательстве стараются не повредить ростковые зоны.
Реабилитационный прогноз и период восстановления
Реабилитационный прогноз у детей обычно благоприятен. Очевидно, что период восстановления будет зависеть от тяжести травмы: если перелом, например, ключицы без повреждения сосудисто-нервного пучка, скорее всего, не оставит после себя никаких последствий, то осложненный компрессионный перелом позвоночника может потребовать множество усилий для восстановления утраченных функций. Осложненный прогноз имеют и переломовывихи, внутрисуставные переломы: часто их следствием становится оссификация (сращение) сустава и ограничение его подвижности.
Процесс восстановления зависит не только от тяжести травмы и возраста пациента, но и от общего состояния организма и сбалансированного питания и подразделяется на три периода:
- Иммобилизационный – с момента оперативного вмешательства до консолидации перелома или формирования рубца, имеющего достаточную прочность. В этот период должны быть созданы благоприятные условия для правильного течения процесса восстановления.
- Постиммобилизационный – с момента снятия иммобилизации до улучшения состояния тканей и восстановления амплитуды движения, силы мышц. Важной задачей в этом периоде является максимальное препятствование сопутствующим нарушениям: атрофии, контрактурам, ригидности суставов и пр.
- Восстановительный – до полного восстановления поврежденного сегмента и восстановления двигательного мастерства.
Каждый период включает в себя несколько значимых задач и способов для их реализации, от которых будет зависеть дальнейший успех.
Занятия в периоде иммобилизации – это профилактика вторичных нарушений, которая включает:
- Идеомоторные упражнения – мысленное представление движения в поврежденном сегменте для профилактики координационных нарушений, сохранения динамического стереотипа.
- Упражнения на свободные от иммобилизации мышечные группы для сохранения подвижности, профилактика атрофии.
- Статические упражнения иммобилизированной конечности для поддержания тонуса мышц.
- Упражнения на противоположной конечности для улучшения трофики.
Занятия в постиммобилизационном периоде направлены на преодоление контрактуры:
- Упражнения на увеличение объема активных движений – профилактика контрактур или же их устранение.
- Механотерапия – добавление пассивного компонента движения.
- Правильное позиционирование конечности способствует профилактике или устранению контрактур.
- Упражнения в воде.
- Криотерапия – противоотечная мера, уменьшение боли. Может использоваться охлажденная вода при заживлении послеоперационной раны, лед в пакете.
Важно помнить, что как раз в периоде постиммобилизации достигается восстановление структурного компонента движения, подвижности, а в восстановительном периоде накладываются различные предметные действия с поврежденной конечностью, достигается утраченное двигательное мастерство или ловкость.
В этом периоде широко используются игровые методы реабилитации, например упражнения с мячом, вовлечение поврежденной конечности в повседневную бытовую активность.
Реабилитация детей после тяжелых переломов
На сегодня только 50% детей, нуждающихся в реабилитации, получают ее в государственных медицинских учреждениях.
У детей реабилитация отличается от нее же у взрослых: часто приходится работать не только с восстановлением утраченных навыков, но и формировать их с нуля – к примеру, многие родители детей младше шести лет жалуются, что после сращения перелома голени ребенка его приходится учить ходить буквально заново. Восстановление после травмы – комплексная задача, затрагивающая не только физические особенности, но и психику маленького пациента. Кроме того, дети нуждаются не только в медицинской, но и в социальной реабилитации. То есть восстановление ребенка после травмы – сложная комплексная задача, включающая медицинские, психологические, педагогические, социальные и физиотерапевтические формы работы. Выпадение любой из них часто ухудшает результат – и это еще одна проблема государственной медицины: жесткие ведомственные разграничения, мешающие координированной работе, которую в идеале должна выполнять мультидисциплинарная бригада специалистов.
Компенсаторные возможности детского организма крайне велики, но большинство специалистов подчеркивает: уже на этапе сопоставления отломков нужно обращаться с поврежденными тканями чрезвычайно бережно, выбирая минимально инвазивные методики – чем обширней вмешательство, тем хуже реабилитационный прогноз. То есть, по сути, медицинская реабилитация пациента начинается еще на этапе лечения, и очень важно не упустить время.
Каадзе Анастасия Геннадьевна Ответственный редактор
Мнение редакции
Реабилитационные центры обязательно должны обеспечивать высокий комфорт проживания маленьких пациентов: жизнеутверждающую эмоциональную атмосферу, игровые комнаты, приветливый персонал, полноценное и разнообразное питание и, конечно, возможность пребывания родителей, бабушек или дедушек на протяжении всего курса реабилитации. Поэтому обязательно контролируйте, какие условия созданы в медучреждении для пребывания ваших детей.
Источник
 20.07.2020
20.07.2020
:
() [1-4]. , , , [5-7].
, , , [8-10].
, – , PubMed, MEDLINE, Ulrichs Periodicals Directory, cyberleninka.ru. 15 .
, , , .
, , 54- . .
, , , , [11-14]. – , , , [15, 16]. , , 0,5-1 10000 [17,18]. , COL1A1 COL1A2, , -, — , , [19-24].
– , 1979 D. Sillence et al. [25], F.H. Gloriex [26] F.S. van Dijk et al. [11]. , , 17 [27], – [28].
, , D. Sillence et al. [25], II III , , [22, 23, 24,29, 30]. , II III , , 8,4 % 27,4 % . , I IV 59,0 13,7 % [31].
C.S. Greeley et al. [32] : II , 2 % , I, III, IV 34 %, 25 %, 35 % 4 % . , , 18,0 [3] 32,0 % [31], 10 % [32].
, , [36-39]. , .. . [40], .. Bourgeois et al. [23] , , 13-14 . M.J. Marion et al. [13] 16 20 . 323 , , , 104 .
61 , , (8 ) (7 ). 17 (27,8 %) [31].
, , , , , [40, 41]. , , [1, 14, 27]. , (100 %), (80 %), (4 %), (24 %), (75 % ). , , [40, 42], [15,16]. 65 % , [43].
, – [44, 45, 46] [47].
, , , , , , [2, 23].
, , , ( ) [21, 41]. [13, 24]. , ‘ , , [48].
, . , , [24, 49, 50]. , , [42, 51]. , R. Cubert et al. [52] , 40 % , , 32 % , , . .. Chen et al. [53] . J. Ruiter-Ligeti et al. [54], 7287994 , , 295 (0,004 %) , , 75 % . , , [55], , , – [29].
‘ , , II , [25, 29, 30]. , [10, 24].
– [37, 38]. [8, 19]. : – : .
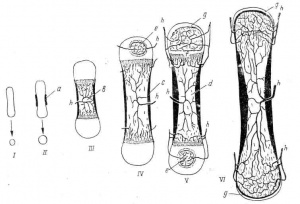
. , , 39 , . – 3740 , – 54 , – 35,5 , – 32 . : 1 – 7 , 5 – 7 .
: 9 – , 18-23 – , 23-27 – , – , 32-39 – .
. 34-35 , , , 6,5 , , (. 1, , ) (. 1, ), .
. 12-13 20-21 – – . , , .
. , – . . . , , ‘ .
( – ): , . , . , . , . . , – . , – , , . .
, . – , (. 2).
, , , . , , -, , , , .
, , : – : , III . , .
II . . . . . .
(. 3)
, , , , . ( ѻ ( ) 0,05 /).
– . . .
16 . . , , .
, , , [36, 38]. , , , . . , , , , , , [2, 13, 23, 40]. , , , . , , , . – , , ( ) .
, , , , [2, 24]. , [6, 7], .
. II III , [22]. , 34-35 .
: , , – ѻ, , , .
, , , . . , . – – [4, 13, 19, 20, 28].
1. Khan M.K., Hossain M.B. A case of brittle bone disease // Mvmensingh Med. J. 2004. Vol. 13, No 2. P.199-200.
2. Severe osteogenesis imperfecta Type-Ill and its challenging treatment in newborn and preschool children. A systematic review / J.J. Sinikumpu, M. Ojaniemi, P. Lehenkari, W. Serlo // Injury’. 2015. Vol. 46, No 8. P. 1440-1446. DOI: 10.1016/].injury.2015.04.021.
3. Yimgang D.P., Brizola E., Shapiro I.R., Health outcomes of neonates with osteogenesis imperfecta: a cross-sectional study // J. Matem. Fetal Neonatal Med. 2016. Vol. 29, No 23. P. 3889-3893. DOI: 10.31094767058.2016.1151870.
4. Collagen defects in lethal perinatal osteogenesis imperfecta / J.F. Bateman, D. Chan, T. Mascara, I.G. Rogers, W.G. Cole // Biochem. J. 1986. Vol. 240, No 3. P. 699-708.
5. (Q 78.0): / . , ; -. – (ATOP); .: .. , .. , .. . , 2013.16 .
6. .., .., .. ( ) // . 2016. 2. . 97-103. DOI 10.18019/1028-4427-2016-2-97-103.
7. Pashenko A. Results of application of intramedullary telescopic fixators in the treatment of long bone deformities of limbs in children with osteogenesis imperfect // Orthopaedics, Traumatology and Prosthetics. 2016. No 3. P. 66-72. DOI 10.15674’t)030-59872016366-72.
8. / .. , .. , .. , .. , .. // . 2011. 1. . 65-69.
9. Brittle bone disease type III in neonates – own experience / E. Jakubowska-Pietkewicz, A. Rusinska, I. Michalus, D. Chlebna-Sokol // Przegl. Lek. 2012. Vol. 69, No 4. P. 139-142.
10. Himakhun W., Rojnueangnit K., Prachukthum S. Perinatal lethal osteogenesis imperfecta in a Thai newborn: the autopsy and histopathological findings // J. Med. Assoc. Thai. 2012. Vol. 95, No Suppl. 1. P. S190-S194.
11. Classification of Osteogenesis imperfecta revisited / F.S. Van Dijk, G. Pals, R.R. van Rijn, P.G. Nikkels, J.M. Cobben/’Eur. J. Med. Genet 2010. Vol. 53, No 1. P.1-5. DOI: 10.1016 j.ejmg.2009.10.007.
12. : / .: .. , .. , .. , .. . [], 2016. URL: https7;’medi.ru klinicheskie-rekomendatsii/nesovershennyj-osteogenez_14106/*part_13. ( : 15.10.17).
13. Skeletal dysplasia in perinatal lethal osteogenesis imperfecta. A complex disorder of endochondral and intramembranous ossification/ M.J. Marion, F.H. Gannon, M.D. Fallon, M.T. Mennuti, R.F. Lodato, F.S. Kaplan !l Clin. Orthop. Relat Res. 1993. No 293. P.327-337.
14. Binder H. Rehabilitation of infants with osteogenesis imperfecta // Connect. Tissue Res. 1995. Vol. 31, No 4. P. S37-S39.
^. : , , , / .. , .. , .. , 1. Khan M.K., Hossain M.B. A case of brittle bone disease // Mvmensingh Med. J. 2004. Vol. 13, No 2. P.199-200.
2. Severe osteogenesis imperfecta Type-Ill and its challenging treatment in newborn and preschool children. A systematic review / J.J. Sinikumpu, M. Ojaniemi, P. Lehenkari, W. Serlo // Injury’. 2015. Vol. 46, No 8. P. 1440-1446. DOI: 10.1016/].injury.2015.04.021.
3. Yimgang D.P., Brizola E., Shapiro I.R., Health outcomes of neonates with osteogenesis imperfecta: a cross-sectional study // J. Matem. Fetal Neonatal Med. 2016. Vol. 29, No 23. P. 3889-3893. DOI: 10.31094767058.2016.1151870.
4. Collagen defects in lethal perinatal osteogenesis imperfecta / J.F. Bateman, D. Chan, T. Mascara, I.G. Rogers, W.G. Cole // Biochem. J. 1986. Vol. 240, No 3. P. 699-708.
5. (Q 78.0): / . , ; -. – (ATOP); .: .. , .. , .. . , 2013.16 .
6. .., .., .. ( ) // . 2016. 2. . 97-103. DOI 10.18019/1028-4427-2016-2-97-103.
7. Pashenko A. Results of application of intramedullary telescopic fixators in the treatment of long bone deformities of limbs in children with osteogenesis imperfect // Orthopaedics, Traumatology and Prosthetics. 2016. No 3. P. 66-72. DOI 10.15674’t)030-59872016366-72.
8. / .. , .. , .. , .. , .. // . 2011. 1. . 65-69.
9. Brittle bone disease type III in neonates – own experience / E. Jakubowska-Pietkewicz, A. Rusinska, I. Michalus, D. Chlebna-Sokol // Przegl. Lek. 2012. Vol. 69, No 4. P. 139-142.
10. Himakhun W., Rojnueangnit K., Prachukthum S. Perinatal lethal osteogenesis imperfecta in a Thai newborn: the autopsy and histopathological findings // J. Med. Assoc. Thai. 2012. Vol. 95, No Suppl. 1. P. S190-S194.
11. Classification of Osteogenesis imperfecta revisited / F.S. Van Dijk, G. Pals, R.R. van Rijn, P.G. Nikkels, J.M. Cobben/’Eur. J. Med. Genet 2010. Vol. 53, No 1. P.1-5. DOI: 10.1016 j.ejmg.2009.10.007.
12. : / .: .. , .. , .. , .. . [], 2016.
13. Skeletal dysplasia in perinatal lethal osteogenesis imperfecta. A complex disorder of endochondral and intramembranous ossification/ M.J. Marion, F.H. Gannon, M.D. Fallon, M.T. Mennuti, R.F. Lodato, F.S. Kaplan !l Clin. Orthop. Relat Res. 1993. No 293. P.327-337.
14. Binder H. Rehabilitation of infants with osteogenesis imperfecta // Connect. Tissue Res. 1995. Vol. 31, No 4. P. S37-S39.
15. : , , , / .. , .. , .. ,H. . , .. // . 2009. . 12, 4. . 38-48.
16. .., .., .. : // . 2015. 2 (22). . 69-73.
17. Fracture Rates and Fracture Sites in Patients With Osteogenesis Imperfecta: A Nationwide Register-Based Cohort Study / L. Folkestad, J.D. Hald, A.K. Ersbol, J. Gram, A.P. Hermann, B. Langdahl, B. Abrahamsen, K. Brixen// J. Bone Miner. Res. 2017. Vol. 32, No 1. P. 125-134. DOI: 10.100Z jbmr.2920.
18. Osteogenesis imperfect / C. Michell, V. Patel, R. Amirfeyz, M. Gargan // Curr. Orthop. 2007. Vol. 21, No 3. P. 236-241. DOI: lO.lOld’J. cuor.2007.04.003.
19. Severe osteogenesis imperfecta caused by double glvcine substitutions near the amino-terminal triple helical region in COL1A2 / M. Takagi, H. Shinohora, S. Narumi, G. Nishimura, Y. Hasegawa, T. Hasegawa//Am. J. Med. Genet A. 2015. Vol. 167, No 7. P. 1627-1631. DOI: 10.1002/ ajmg.a.37051.
20. Cheung M.S., Glorieux F.H. Osteogenesis Imperfecta: up on presentation and management H Rev. Endocr. b. Disord. 2008. Vol. 9, No 2. P. 153-160. DOI: 10.1007/sl 1154-008-9074-4.
21. The clinicopathological features of three babies with osteogenesis imperfecta resulting from the substitution of glycine by valine in the pro alpha 1 (I) chain of type I procollagen/W.G. Cole, E. Patterson, J. Bonadio, P.E. Campbell, D.W. Fortune// J. Med. Genet.1992. Vol. 29, No 2. P.112-118.
22. Prenatal diagnosis of osteogenesis imperfecta. Two cases /1. Baalbakv, S. Manouvrier, P. Dufour, L. Devismes, A. Delzenne, O. Boute, F. Puech // I. Gynecol. Obstet Biol. Reprod. 1998. Vol. 27, No 1. P. 44-51.
23. Osteogenesis imperfecta: from diagnosis and multidisciplinary treatment to future perspectives/A. Bregou Bourgeois, B. Aubrv-Rozier, L. Bonafe, L. Laurent-Applegate, D.P. Pioletti, P.Y. Zambelli // Swiss Med. Wkly. 2016. Vol. 146. P. wl4322. DOI: 10.4414/smw.2016.14322.
24. Recent developments in osteogenesis imperfecta / J.L. Shaker, C. Albert, J. Fritz, G. Harris // FlOOORes. 2015. Vol. 4, F 1000 Faculty Rev. P. 681. DOI: 10.12688/fl OOOre.6398.1.
25. Sillence D.O., Senn A., Danks D.M. Genetic heterogeneity in osteogenesis imperfecta H J. Med. Genet 1979. Vol. 16, No 2. P.101-116.
26. Glorieux F.H. Osteogenesis imperfecta // Best Pract. Res. Clin. Rheumatol. 2008. Vol. 22, No 1. P. 85-100. DOI: 10.1016 /j.berh.2007.12.012.
27. Bishop N. Characterising and treating osteogenesis imperfecta // Early Hum. Dev. 2010. Vol. 86, No 11. P. 743-746. DOI: 10.1016/j. earlhumdev.2010.08.002.
28. Van Dijk F.S., Sillence D.O. Osteogenesis imperfecta: clinical diagnosis, nomenclature and severity assessment//Am. J. Med. Genet. A. 2014. Vol. 164A, No 6. P. 1470-1481.
29. Lethal osteogenesis imperfecta in a Congolese newborn infant / G. Moven, J.L. Nkoua, M. Pongui, A.M. Mafouta, S. Nzingoula /7 Arch. Fr. Pediatr. 1993. Vol. 50, No 10. P. 891-893.
30. Perinatal lethal type II osteogenesis imperfecta: a case report/I.D. Ayadi, E.B. Hamida, R.B. Rebeh, S. Chaouachi, Z. Marrakchi // Pan Afr. Med. J. 2015. Vol. 21. P. 11.
31. : /. , .. –, .. , .. // . 2016. . 13, 1. . 44-43. DOI 10.15690/pf.vl3i 1/.514.
32. Fractures at diagnosis in infants and children with osteogenesis imperfect/ C.S. Greeley, M. Donaruma-Kwoh, M. Vettimattam, C. Lobo, C. Williard, L. Mazur//1. Pediatr. Orthop. 2013. Vol. 33, No 1. P. 32-36. DOI: 10.1097,BPO.0b013e318279c55d.
33. Neonatal clavicular fracture: recent 10 vear studv / E.S. Ahn, M.S. Jung, Y.K. Lee, S.Y. , S.M. Shin, M.H. Hahn // Pediatr. Int. 2015. Vol. 57, No 1. P. 60-63. DOI: 10.1111/ped.l2497.
34. Mane P.P., Challawar N.S., Shah H. Late presented case of distal humerus epiphyseal separation in a newborn //BMJ Case Rep. 2016. Vol. 2016. P. bcr2016215296. DOI: 10.1136/bsr-2016-215296.
35. Birth-associated femoral fractures: incidence and outcome / S. Morris, N. Cassidy, M. Stephens, D. McCormack, F. McManus// J. Pediatr. Orthop. 2002. Vol. 22, No 1. P.27-30.
36. Osteochondrodysplasias. Prenatal diagnosis and pathological-anatomic findings / C. Tennestedt, S. Bartho, R. Bollmann, A. Schwenke, I. Nitz, K. Rothe H Zentralbl. Pathol. 1993. Vol. 139, No 1. P.71-80.
37. Hackley L., Merritt L. Osteogenesis imperfecta in the neonate // . Neonatal Care. 2008. Vol. 8, No 1. P. 21-30. DOI: 10.1097/01. ANC.0000311013.71510.41.
38. Chalubinski K., Schaller A. Prenatal diagnosis of osteogenesis imperfecta. Report of a case classified as the classical Ekman Lobstein type Ultraschall. Med. 1994. Vol. 15, No 1. P. 38-42. DOI: 10.1055/s-2007-1004003.//Am. J. Med. Genet.1984. Vol. 19, No 4. P. 707-714. DOI: 10.1002/ajmg.l320190410.
40. /.. , . , .. , .. . 2009. 2 (28). . 138-140.
41. / .. , .. , .. , .. // . 2008. 2 (19). . 92-95.
42. : , /.. , .. , .. , .. -, .. , .. // . 2015. 37. . 47-51.
43. .., – .., .. , : . 2015. . 12, 5. . 579-588. DOI 10.15690/pf.vl2i5.1461.
44. / .. , .. , .. , .. -, .. //- . 2012. 3. . 67-70.
45. Infantile spinal muscular atrophy variant with congenital fractures in a female neonate: e%ridence for autosomal recessive inheritance/W. Courtens, A.B. Johansson, B. Dachy, F. Avni, N. Telerman-Toppet, H. Scheffer// J. Med. Genet. 2002. Vol. 39, No 1. P.74-77.
46. Neonatal fractures as a presenting feature of LMOD3-associated congenital myopathy / M. Abbott, M. Jain, R. Pferdehirt, Y. Chen, A. Tran, M. B. Duz, M. Seven, R.A. Gibbs, D. Muzny, B. Lee, R. Marora, L.C. Burrage//Am. J. Med. Genet. A. 2017. Vol. 173, No 10. P. 2789-2794. DOI: 10.100Z”ajmg.a.38383.
47. Lethal osteopetrosis with multiplae fractures in utero / N. el Khazen, D. Faverly, E. Vamos, N. van Regemorter, J. Flament-Durand, B. Carton, N. Cremer-Perlmutter//Am. J. Med. Genet. 1986. Vol. 23, No 3. P. 811-819. DOI: 10.100Z’ajmg.l320230308.
48. Subperiosteal new bone and callus formations in neonates with femoral shaft fracture at birth / T. Hosokawa, Y. Yamada, Y. Sato, Y. Tanami, E. Oguma // Emerg. Radiol. 2017. Vol. 24, No 2. P.143-148. DOI: 10.1007/sl0140-016-1462-6.
49. Osteogenesis imperfecta: cesarean deliveries in identical twins /. Dinges, C. Ortner, L. Bollag, J. Davies, R. Landauii Int. J. ObsteL Anesth. 2015. Vol. 24, No 1. P. 64-68.
50. Quakemack K., Beckmann M., de Moll H. Osteogenesis imperfecta in pregnancy//Geburtshilfe Frauenheilkd. 1980. Vol. 40, No 2. P. 180-184. DOI: 10.1055/S-2008-1037215.
51. Cesarean delivery is not associated with decreased at-birth fracture rates in osteogenesis imperfecta / S. Bellur, M. Jain, D. Cuthbertson, D. Krakow, J.R. Shapiro, R.D. Steiner, P.A. Smith, M.B. Bober, T. Hart, J. Krischer, M. Mullins, P.H. Byers, M. Pepin, M. Durigova, F.H. Glorieux, F. Rauch, V.R. Sutton, B. Lee, Members of the BBD Consortium, S.C. Nagamani// Genet. Med. 2016. Vol. 18, No 6. P. 570-576. DOI: 10.1038/gim.2015.131.
52. Osteogenesis imperfecta: mode of delivery and neonatal outcome / R. Cubert, E.Y. Cheng, S. Mack, M.G. Pepin, P.H. Byers // Obstet. Gvnecol. 2001. Vol. 97, No 1. P. 66-69.
53. Uncomplicated vaginal delivery in two consecutive pregnancies carried to term in a woman with osteogenesis imperfecta type I and bisphosphonate treatment before conception/ C.P Chen, S.P. Lin, Y.N. Su, J.P Huang, S.R. Chem, J.W. Su, W. Wang//Taiwan J. Oostet. Gynecol. 2012. Vol. 51, No 2. P. 305-507. DOI: 10.1016/j.tjog.2012.04.029.
54. Pregnancy outcomes in women with osteogenesis imperfecta: a retrospective cohort study / J. Ruiter-Ligeti, N. Czuzoj-Shulman, A.R. Spence, T. Tulandi, H.A. Abenhaim // J. Perinatol. 2016. Vol. 36, No 10. P. 828-831. DOI: 10.1038/jp.2016.111.
55. Anderer G., Hellmever L., Hadji P. Clinical management of a pregnant patient with type I osteogenesis imperfecta using quantitative ultrasonometry -a case report // Ultraschall. Med. 2008. Vol. 29, No 2. P. 201-204. DOI: 10.1055/s-2006-927241.
56. 6– /.. , .. , .. , .. , .. , .. , .. //, . 2017. . 5, 2. . 52-58. DOI 10.17816/PTORS5252-58.
57. / .. , .. , .. , .. , .. , .. , .. , .. , .. . 2017. . 18, N- 2 (90). . 83-86.
58. () / .-.: .. , .. , .. , .. , .. , .. , .. , .. , .. , .. , .. , .. , .. . [. .]. 40 . URL: /..,-1/1&,2017/03/ ———–.(
59. Osteogenesis imperfecta / J.C. Marini, A. Forlino, H.P. Bachinger, N.J. Bishop, PH. Byers, A. Paepe, F. Fassier, N. Fratzl-Zelman, K.M. Kozloff, D. Krakow, K. Montpetit, O. Sender//Nat. Rev. Dis. Primers. 2017. Vol. 3. P.17052. DOI: 10.1038/nrdp.2017.52.
60. Safety and efficacy of a 1-year treatment with zoledronic acid compared with pamidronate in children with osteogenesis imperfecta / E.R. Barros, G.L. Saraiva, T.P. de Oliveira, M. Lazaretti-Castro//J. Pediatr. Endocrinol. b. 2012. Vol. 25, No 5-6. P. 485-491.
1. , . . ., , , . ,
2. , , . ,
3. , 2
4. , . . ., , . , , , . ,
5. , . . ., , . , , 2
6. , . . ., , . ,
7. , . . ., 2, , . ,
8. , …, ӫ֫λ …. ,.,
:
234567 :
234567 (): 20.07.2020 15:49:00
234567 (ID): 989
234567 : , ,
12354567899
Источник
