Сармиенто лечение переломов
Lorenz Böhler в 1964 г. писал: «Перелом диафиза плечевой кости является самым благоприятным из диафизарных переломов длинных трубчатых костей. При правильном наложении повязки… такие переломы практически всегда просто излечиваются консервативными средствами» [1]. Тем не менее, следует отметить, что консервативное лечение, как и хирургическое, требует четкой концепции и соответствующего контроля на всех его этапах, и его вовсе не следует рассматривать как «беспроблемное».
Ранее крайне редкие показания к хирургическому лечению в течение последних 50 лет значительно расширились. Так, по данным исследований Ассоциации остеосинтеза (АО), в 1991 г. около 50% диафизарных переломов плечевой кости лечились хирургическими методами [8].
Анатомические особенности
В плечевой кости выделяют проксимальный и дистальный эпифизы и диафизарную часть. Дистальный конец плечевой кости развернут кнутри относительно проксимального в среднем на 16º (торсия диафиза плечевой кости). Диафиз плечевой кости в проксимальном отделе имеет округлую в сечении форму, дистальнее уплощается и становится треугольным. Диафизарная часть плеча со всех сторон покрыта мышечными тканями: сгибателями предплечья (двуглавая и плечевая мышцы) и разгибателями (трехглавая мышца плеча).
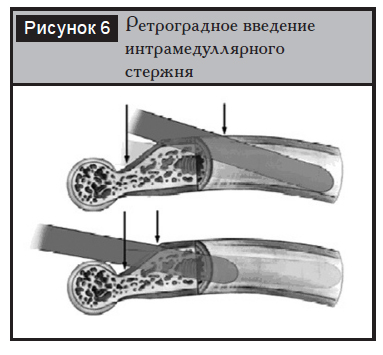
Лучевой нерв проходит спиралеобразно по задней поверхности плечевой кости в средней трети, затем переходит на переднелатеральную поверхность, прободевая межмышечную перегородку, которая является зоной относительной фиксации нерва. Согласно исследованиям R.?Zobrist [10], данная точка располагается на расстоянии 11,9?±?1,0?см от наружного надмыщелка (рис. 1). При этом положение нерва не зависело от сгибания или разгибания в локтевом суставе, а также от приведения или отведения в плечевом суставе; изменялась лишь степень натяжения нерва. Наличие такой фиксации может приводить к повреждениям нерва во время перелома, а также при манипуляциях (репозиция, рассверливание костномозгового канала и др.).
Эпидемиология повреждений
Одно из наиболее репрезентативных исследований эпидемиологии проведено G.?Tytherleigh-Strong из Эдинбурга [9]. В исследовании принимали участие 249 пациентов с диафизарными переломами плечевой кости, наблюдавшихся в течение трехлетнего периода. Были определены морфология повреждений, механизмы травмы, распределение больных по полу и возрасту. В 63% случаев наблюдались простые переломы (типа А по классификации АО), в 26,2% отмечены оскольчатые переломы типа В, в 10,2% случаев – раздробленные типа С. 60% переломов располагались в средней трети диафиза плечевой кости, 30% – в проксимальной трети, 10% – в дистальной. Открытые переломы составили менее 10%. Распределение пациентов по возрасту показало два пика заболеваемости: первый – у мужчин на третьем десятилетии жизни при средне- или высокоэнергетичной травме, второй – более выраженный?– у женщин старше 70 лет, как правило, после простых падений.
Диагностика
Клиническая диагностика перелома диафиза плечевой кости основывается на локальной болезненности и характерном щажении конечности и прижатии ее к грудной клетке. При политравме или у пациента в бессознательном состоянии при общем клиническом обследовании выявляется патологическая подвижность в зоне перелома. При первичном осмотре следует обращать также внимание на состояние мягких тканей, чтобы предупредить возможный прокол кожи изнутри либо дополнительную контаминацию при открытом переломе.
Особое значение при переломах плечевой кости имеет неврологическое обследование, а именно целенаправленное изучение состояния лучевого нерва. При дистальных переломах плечевой кости возможно также повреждение локтевого нерва. Повреждение сосудов проявляется отсутствием пульса на а. radialis и служит показанием к ангиографии или допплеровскому исследованию.
Рентгенологическое исследование поврежденного сегмента конечности в двух проекциях является достаточным для определения типа перелома и формирования плана дальнейшего лечения.
Цель лечения перелома?– полное восстановление функции пораженной конечности. При выборе метода лечения следует учитывать тип повреждения, наличие сопутствующих травм или заболеваний, социальный статус пациента, профессию, доминирующую конечность (правая/левая), наличие ожирения.
Консервативное лечение
Стандартным методом консервативного лечения в нашей стране является применение гипсовой повязки по Волковичу в виде длинной лонгеты, накладываемой от здорового надплечья до кисти травмированной конечности на срок от 6 до 12 недель. Данная повязка позволяет достаточно эффективно устранять угловые смещения отломков, однако является весьма неудобной и обременительной для пациента.
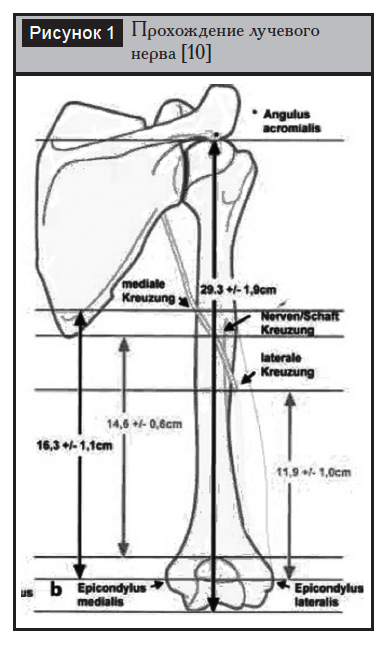
Другим методом консервативного лечения является применение функциональных повязок по Sarmiento [7]. Условиями его применения являются низкий уровень болезненности и способность пациента активно сгибать и разгибать конечность в локтевом суставе. Состояние мягких тканей и габитус больного также должны соответствовать определенным требованиям, например ожирение является относительным противопоказанием к применению данного метода из-за высокой опасности сращения с варусным отклонением дистального отломка.
Первично в течение 7–10 дней применяется длинная гипсовая шина в положении сгибания в локтевом суставе на 90°. Затем накладывается короткая «гильза», оставляющая свободными локтевой и плечевой суставы. В соответствии с клиническими и рентгенологическими признаками консолидации данная шина применяется в среднем до 12 недель с момента травмы (рис. 2). Допустимыми смещениями при консервативном лечении считаются укорочение до 1 см, поперечные смещения до ширины диафиза и угловые отклонения до 25º [7].
А.?Sarmiento и соавт. сообщают о результатах лечения 620 пациентов в период с 1978 по 1990 г. Помимо 465 закрытых переломов имелось 155 открытых (25%). При первичном неврите лучевого нерва (67 человек, 11%) выполнялся невролиз с последующим консервативным лечением перелома. Консолидация достигнута у 604 пациентов, у 16 отмечено несращение.
Тем не менее, эти результаты нельзя слепо переносить на европейские условия. Так, средний возраст больных составил 36 лет, а об опыте или особенностях применения данного метода лечения в условиях возрастного остеопороза авторы не сообщают. Помимо этого у абсолютного большинства пациентов (98%) к моменту окончания лечения отмечались значительные ограничения объема движений в прилежащих суставах.
Хирургическое лечение
С учетом того, что консервативное лечение при правильном применении позволяет достичь хороших результатов у большинства пациентов, показания к хирургическому лечению устанавливаются в индивидуальном порядке.
Показания к хирургическому лечению диафизарных переломов плечевой кости согласно F.?Bonnaire et al. [2]:
1. Абсолютные показания: политравма; открытый перелом; повреждение сосудов; флоттирующее плечо/локоть; переломы плечевых костей с обеих сторон.
2. Относительные (рекомендуемые) показания: короткие косые и поперечные переломы; проксимальные или дистальные переломы; личные обстоятельства и желание пациента; невправляемые переломы; несращения.
Среди методов хирургического лечения наибольшее распространение получили открытая репозиция и остеосинтез пластиной, интрамедуллярный остеосинтез, а также применение аппаратов внеш-ней фиксации.
Остеосинтез пластиной
Доступы. Основными доступами являются переднелатеральный и задний доступ по Henry.
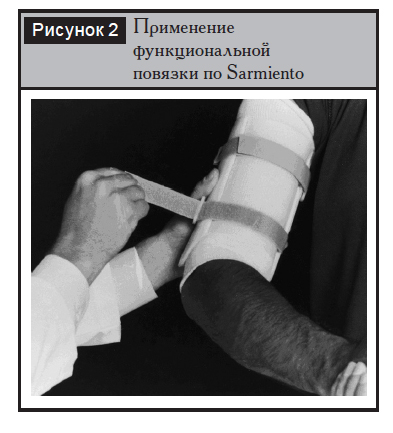
Переднелатеральный доступ чаще применяется при переломах верхней и средней третей плеча, однако при необходимости он может быть расширен на всю длину плечевой кости. Чем более проксимально располагается перелом, тем чаще приходится отсекать дельтовидную мышцу в зоне ее прикрепления. После выделения плечевой мышцы последняя расслаивается вдоль хода ее волокон по границе средней и наружной третей. Таким образом лучевой нерв после прохождения межмышечной перегородки защищается волокнами плечевой мышцы (рис. 3, а, б).
Задний доступ применяется при переломах средней и дистальной третей диафиза плечевой кости в положении больного на животе либо на боку со сгибанием в локтевом суставе более 90º и свободным положением предплечья. Выполняется продольный разрез по задней поверхности плеча, после рассечения поверхностной фасции пальпируется борозда между двумя поверхностными головками трехглавой мышцы, которые тупо разволокняются между собой. В глубине между головками мышцы выявляется лучевой нерв (рис. 3, в).
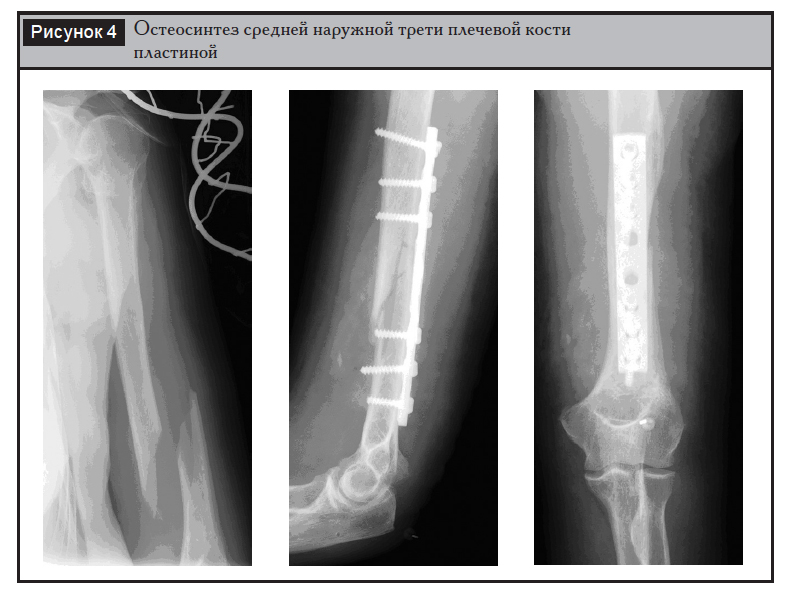
Выбор имплантата. У большинства больных имплантатом выбора является широкая 4,5?мм пластина с ограниченным контактом (LCP, LC-DCP). У субтильных пациентов (пациенток) возможно использование узкой 4,5?мм пластины, в редких случаях применима 3,5?мм система имплантатов (рис. 4). Фиксация каждого из основных фрагментов перелома должна осуществляться как минимум тремя винтами (6 кортикальных слоев). При косых и спиральных переломах при возможности применяется межфрагментарная компрессия винтами. При многооскольчатых переломах используется техника биологического остеосинтеза с фиксацией только основных фрагментов без выделения промежуточных осколков. Лучевой нерв часто проходит над пластиной, особенно при заднем доступе, по-этому в протоколе операции необходимо указывать его положение на момент завершения операции относительно отверстий пластины [2].
Интрамедуллярный остеосинтез
В отличие от диафизарных переломов бедра и голени, где интрамедуллярный остеосинтез давно стал стандартным методом лечения, при переломах плечевой кости данный метод лишь завоевывает свое место в арсенале травматологов. Этому способствует появление имплантатов, специально разработанных с учетом специфической анатомии костномозгового канала плечевой кости. При многих переломах, прежде всего на фоне остеопороза, а также при коротких косых или поперечных переломах интрамедуллярный остеосинтез имеет преимущества перед использованием пластин. Противопоказанием к интрамедуллярному остео-синтезу служат переломы дистального отдела плечевой кости.
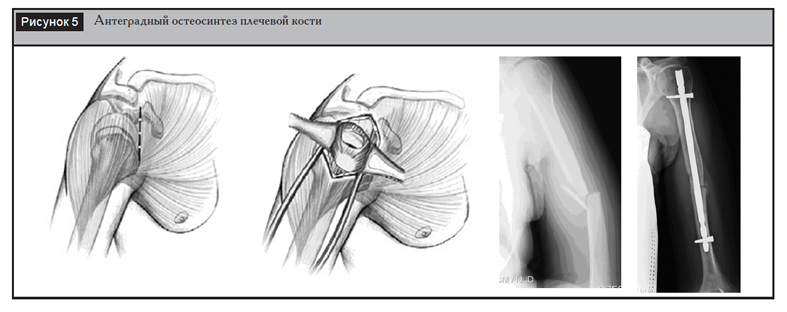
Антеградный остеосинтез плечевой кости осуществляется, как правило, в положении «пляжного кресла». Выполняется разрез кожи длиной 2–5 см по переднелатеральной поверхности дель-товидной области с последующим продольным разволокнением дельтовидной мышцы. Выделяются сухожилия ротаторной манжеты и рассекаются продольно ходу их волокон в области большого бугорка (рис. 5). Вскрытие костномозгового канала осуществляется специальным шилом, после чего водится внутренний фиксатор.
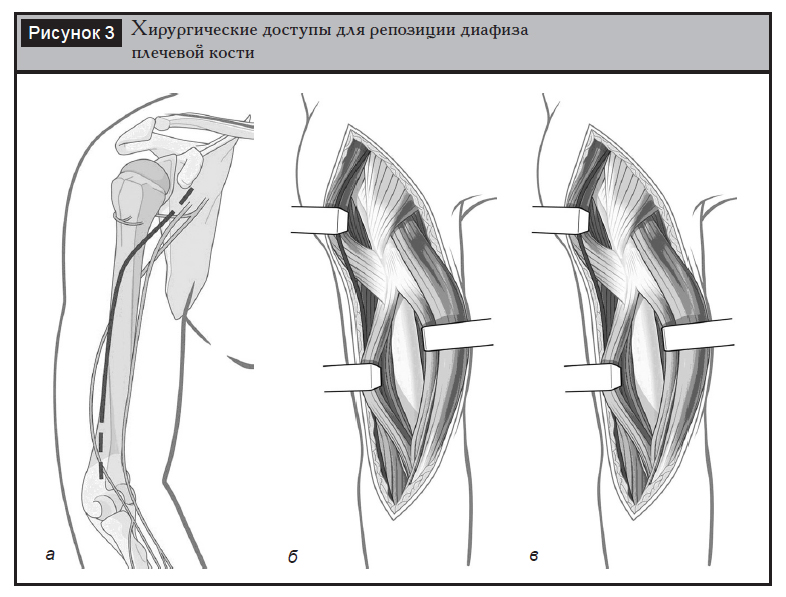
При ретроградном остеосинтезе, выполняемом в положении пациента на животе, точка введения конструкции находится чуть проксимальнее ямки локтевого отростка. Выполняется продольный разрез кожи длиной 6–7 см с разволокнением трехглавой мышцы плеча до кости. Точка введения имплантата тщательно подготавливается ввиду нередких осложнений в виде переломов дистального отдела плечевой кости (рис. 6).

Общим преимуществом интрамедуллярного остеосинтеза плечевой кости является меньшая инвазивность по сравнению с остеосинтезом пластиной, хотя как проксимальный доступ через ротаторную манжету, так и дистальный через ямку локтевого отростка могут сопровождаться специфическими осложнениями (см. ниже).
Внешняя фиксация
Основным показанием к применению внешней фиксации при переломах плечевой кости является лечение перелома плеча у пациентов с множественными повреждениями (политравма) или значительное повреждение мягких тканей. Помимо этого метод применим при возникновении инфекционных осложнений погружного остеосинтеза. Недостатки внешней фиксации (спицевая/стержневая инфекция, замедленное сращение, неудобства для пациента) ограничивают показания к ее применению.
Осложнения
Фиксация пластиной. Открытая репозиция и внутренняя фиксация диафизарных переломов плеча сопровождаются минимальным уровнем осложнений. В целом уровень нагноений или несращений составляет около 1–2% случаев.
Интрамедуллярная фиксация. Уровень инфекционных осложнений при интрамедуллярном остеосинтезе обычно низок. Однако частота болей в точке введения в разных сообщениях варьируется от 0 до практически 100%. Общепринято, однако, что сохранение относительно аваскулярной зоны ротаторной манжеты при введении гвоздя и его погружение примерно на 5 мм ниже уровня суставного хряща позволяют значительно снизить болезненность в точке введения. При ретроградном остеосинтезе проблемы в точке введения могут включать боли в локтевом суставе, контрактуры, гетеротопическую оссификацию и перелом из-за концентрации напряжения вслед-ствие эксцентричности расположения точки введения. Дополнительно ослаблять дистальный отдел плечевой кости может проведение блокирующих винтов в латеромедиальном направлении.
Уровень замедленной консолидации или несращений колеблется от 0 до 29%. Частота этих осложнений может быть снижена предупреждением чрезмерного рассверливания, тщательной установкой блокирующих винтов и, что самое важное, предупреждением перерастяжения перелома [5, 6].
Первичное повреждение лучевого нерва
Частота первичных повреждений лучевого нерва составляет в среднем около 11%, однако при переломах дистального отдела плеча может достигать 30%. Последние исследования показывают, что при высокоэнергетичных повреждениях с варусным смещением дистального отломка повреждение лучевого нерва происходит чаще.
Подход к лечению повреждений лучевого нерва является предметом острых споров, при этом существуют две конкурирующие концепции:
1) выжидательная тактика с консервативным лечением перелома. Согласно данным L.?Böhler, 80–90% первичных парезов лучевого нерва восстанавливаются спонтанно. При отсутствии восстановления функции в срок более 6 мес. после травмы показана поздняя ревизии нерва;
2) первичная ревизия нерва с одновременным остеосинтезом, так как около 10–20% случаев пареза лучевого нерва не проходят спонтанно [9].
Отсутствие единой тактики лечения таких повреждений требует индивидуального подхода к лечению конкретного пациента, тем не менее, на современном этапе отмечается тенденция к более широкому применению ревизии нерва с одновременным остеосинтезом.
Вторичные повреждения нерва при консервативном лечении крайне редки и связаны в основном с каллезными изменениями окружающих нерв тканей. При этом показан невролиз нерва, который, однако, технически сложен.
Послеоперационные повреждения лучевого нерва встречаются примерно в 3% случаев, при этом большинство авторов однозначно рекомендуют раннюю ревизию нерва (если он не был надежно визуализирован при первичной операции) [2, 3, 8].
Таким образом, значительная часть диафизарных переломов плечевой кости может быть излечена консервативными средствами. Показания к хирургиче-скому лечению при данных повреждениях устанавливаются в индивидуальном порядке с учетом активности пациента, типа повреждения и сопутствующей патологии. Открытая репозиция и фиксация переломов пластиной является в настоящее время стандартом хирургического лечения, особенно при распространении на дистальные отделы, повреждениях нервов или сосудов. Интрамедуллярный остеосинтез приобретает большее распространение в последние годы, особенно при поперечных, а также многооскольчатых переломах [4].
ЛИТЕРАТУРА
1. Böhler L. // Langenbecks Arch. Klin. Chir.?– 1964.?– Vol.?308.?– P.?465–475.
2. Bonnaire F., Götze B., Schlickewei W., Zenz M. // Akt Traumatol. – 2001.?– Vol.?31.?– P.?82–89.
3. Brug E., Joist A., Meffert R. // Unfallchirurg.?– 2002.?– Vol.?105.?– P.?82–85.
4. Chapman J.R., Henley M.B., Agel J. et al. // J. Orthop. Trauma.?– 2000.?– Vol.?14.?– P.?162–166.
5. Crates J., Whittle A.P. // Clin Orthop.?– 1998.?– Vol.?350.?– P.?40–50.
6. Rommens P.M., Kuechle R., Bord Th. // Injury, Int. J. Care Injured.?– 2008.?– Vol.?39.?– P.?1319–1328.
7. Sarmiento A., Zagorsky J.B., Zych G.A. et al. // J. Bone Joint Surg. Am.?– 2000.?– Vol.?82.?– P.?478–486.
8. Schittko A. // Unfallchirurg.?– 2003.?– Vol.?106.?– S.?145–160.
9. Tytherleigh-Strong G., Walls N., McQueen M.M. // J. Bone Joint Surg. Br.?– 1998.?– Vol.?80.?– P.?249–253.
10. Zobrist R., Messmer P., Levin L.S., Regazzoni P. // Unfallchirurg.?– 2002.?– Vol.?105.?– S.?246–252.
Медицинские новости. – 2010. – №12. – С. 35-38.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.
Источник
До начала 1980-х годов основными методами консервативного лечения являлись одномоментная репозиция с наложением высокой гипсовой повязки и метод скелетного вытяжения с последующей гипсовой иммобилизацией. Каждый из них имеет свои минусы. При первом — существует опасность нарастания отека с развитием компартмент-синдро-ма и вторичного смещения отломков после спадения посттравматического отека. При втором — больной на протяжении 3—3,5 недель прикован к кровати и, кроме того, нет гарантии, что при замене вытяжения на гипс также не наступит вторичное смещение. Уверен, что каждый из вас многократно сталкивался с подобными случаями.
Ситуация во многом изменилась с внедрением в практику консервативного функционального метода лечения по Сармиенто. Прообраз метода применялся уже в древнем Китае и был возрожден Dehne, Sarmiento и Latta [120]. Sarmiento et al. [122] писали, что на сращение перелома влияют многие факторы: кровоснабжение, механические усилия, химия, электричество, теплопроводность, но «главным из них являются движения в месте перелома, которые ведут к длительной воспалительной реакции, способствущей улучшению кровообращения и, таким образом, ускорению сращения».
Биомеханическая сущность метода заключается в фиксирующей роли мягких тканей, удерживающих отломки в правильном положении, благодаря присущим тканям свойствам упругости и несжимаемости. Е. А. Кашигина с соавт.* так сформулировали биомеханику метода: «Sarmiento A., Latta L. (1981) представляют мышечные ткани, окружающие сломанную кость, как полостную гидравлическую систему, окруженную эластичной кожно-фасциаль-ной оболочкой. Динамическая осевая нагрузка деформирует эту полость, растягивая внешние, фасциальные границы, вызывая смещение костных фрагментов по длине. Снятие нагрузки возвращает отломки в прежнее положение. Жесткие границы гидравлической системы-функциональная гипсовая повязка» (с. 52) [120].
Этот метод получил широкое распространение и в нашей стране. Как это часто бывает при поверхностном знакомстве с тем или
*Е. А. Кашигина, В. М. Панфилов, Е. А. Никифорова. Функциональное лечение диафизарных переломов голени / Вестник Российского Государственного медицинского университета. Специальный выпуск. 2003, 5(31), с. 51-55.
иным способом лечения, этот прогрессивный способ стал применяться при переломах разного характера без учета степени его стабильности.
Травматолог усвоил, что функциональный метод заключается в наложении короткой гипсовой повязки с козырьком над надколенником и гипсовым каблуком по оси больше-берцовой кости (рис. 4.2). Ранняя нагрузка в такой повязке без учета особенностей перелома нередко приводила к вторичному смещению с укорочением конечности и значительными угловыми деформациями. Многие переломы не срастались. Так можно дискредитировать любой способ лечения.
Сами авторы метода очень строго подходят к показаниям к его применению. Они пишут: «Функциональный «bracing» является эффективным способом лечения тщательно отобранных переломов голени, плеча и локтевой кости, главным образом от низкоэнергетических травм. Что касается переломов голени, то метод пригоден только (подчеркнуто мной. — С. Г.) для вправленных поперечных переломов и для переломов с осевой нестабильностью при допустимых степенях укорочения» [120]. Что такое допустимые смещения, по мнению авторов? Это угловое смещение в пределах 5° и смещение по длине, не превышающее 10 мм.
Метод функционального лечения укороченными гипсовыми повязками может применяться сразу при поступлении больного (при переломах без смещения и при стабильных переломах с удавшейся одномоментной репозицией) или после начала формирования провизорной мозоли на вытяжении, в первичном аппарате наружной фиксации или после иммобилизации высокой гипсовой повязкой.
Hackstock H. [121] также отмечает, что этот метод при переломах голени должен применяться только по самым строгим показаниям, которые определяются характером и локализацией перелома. «Хорошие результаты могут быть получены только (подчеркнуто мной. — С. Г.) при стабильных переломах и ранней нагрузке на ногу. Все нестабильные переломы должны фиксироваться высокой гипсовой повязкой на первые 4-6 недель, которая может быть затем заменена на функциональную на следующие 4-6 недель». Kyro et al. [123] считают, что существуют переломы голени, при которых метод Сарми-енто-Латта применяться не должен. К ним они относят очень частые винтообразные переломы в нижней трети голени.
Должен признать, что и в нашей клинике показания к применению функционального метода лечения неоправданно расширялись. Доказательством считаю тот факт, что из 190 больных, которым был применен функциональный метод лечения, 105 — имели винтообразные или винтообразные ос-кольчатые переломы, наименее подходящие для лечения этим способом. С моей точки зрения, это совсем не простой метод, и он требует внимательного и постоянного наблюдения за больным. Необходима «обратная связь», и пациент должен постоянно информировать лечащего врача о своих ощущениях при ходьбе и нагрузке: степени подвижности фрагментов в повязке, наличии боли при нагрузке, появлении углообразной деформации в месте перелома и т.д. Только тогда удается получить неосложненное сращение перелома, которое авторы метода достигли в 97% случаев [120].
При первичном лечении диафизарного перелома методом скелетного вытяжения также существуют подводные рифы, которые могут свести на нет все усилия травматолога. Необходимо стремиться к максимально быстрой репозиции перелома. Только устранение грубого смещения фрагментов может привести к быстрой нормализации периферического кровотока (сосудистый спазм), способствовать быстрому спадению отека.
Поэтому после анестезии места перелома и наложения вытяжения за пяточную кость или надлодыжечную область (реже), дежурный врач должен контролировать правильность положения ноги на вытяжении, увеличить груз на протяжении первых 3-4 ч, а затем уменьшить его после проведения рентгенологического контроля. В ряде случаев необходима и дополнительная первичная ручная репозиция на вытяжении. Одной из наиболее частых причин антекурвации является излишне туго натянутый гамак под голенью на функциональной шине. В таких случаях гамак должен быть перебинтован, соответственно объему икроножной области. Необходимо стремиться к тому, чтобы
больной был «сдан» лечащему врачу уже с репетированным переломом.
Постоянное внимание должно быть уделено нарастанию посттравматического отека голени для того, чтобы не пропустить начало развития компартмент-синдрома. Я о нем скажу ниже. Уже при поступлении больного должны быть выявлены и зафиксированы в истории болезни нарушения кровообращения и иннервации (чаще повреждения малоберцового нерва).
Нередко причиной воспалительных изменений вокруг спицы для вытяжения являются ее недостаточное натяжение и отсутствие фиксации в местах входа и выхода. Внимательное отношение к этому этапу проведения скелетного вытяжения практически гарантирует больному возможность избежать подобных осложнений. В среднем срок скелетного вытяжения 24 дня. За этот срок больному удается оторвать ногу (без груза!) от шины, что наряду с рентгенологическими данными свидетельствует о формировании первичной (иммобилизационной) мозоли. Дальнейшее лечение зависит от характера перелома: нестабильные переломы (винтообразные и длиннокосые, с крупным треугольным клином) требуют наложения высокой гипсовой повязки на срок до сращения перелома. При переломах типа A3, С2 и СЗ может быть применен функциональный метод лечения.
Опасения некоторых травматологов в отношении отрицательного влияния длительной иммобилизации гипсовой повязкой на функцию суставов резко преувеличены. Даже длительная иммобилизация высокой повязкой обычно не приводит к тугоподвижности неповрежденный коленный и голеностопный суставы. В то же время, необходимо максимально избегать такой иммобилизации в случаях, когда выявляется любая травма коленного сустава (гемартроз).
Во многом сложившееся в последнее время отрицательное отношение к консервативному методу связано с утратой необходимых навыков при лечении этими методами. Покажу это на одном примере. Ю. П. Колесников с соавт. [4] изучили результаты консервативного лечения 96 больных с закрытыми диафизарными переломами голени. У 15 больных была применена одномоментная репозицияс наложением гипсовой повязки, а 81 — лечился при помощи скелетного вытяжения.
Отличные и хорошие результаты были получены в 64%, удовлетворительные — в 30% и неудовлетворительные — в 6% наблюдений. А вот какие ошибки и осложнения в процессе лечения выявили авторы: низкую эффективность репозиции скелетным вытяжением из-за нарушений техники, оставшееся ротационное смещение, неумение устранить угловые смещения; в процессе лечения в 16,4% случаев было не диагностировано вторичное смещение отломков, выявлены дефекты в технике наложения гипсовых повязок; необоснованно рано прекращалось скелетное вытяжение и другие ошибки.
Авторы у 29,8% больных нашли длительно существующие контрактуры суставов, а у 28,8% — позднее или неполноценное восстановление функции поврежденной конечности. Ю. П. Колесников с соавт. делают вывод о том, что консервативные методы лечения не обеспечивают необходимого качества лечения и требуют усовершенствования. Такой вывод мне кажется излишне категоричным. Подобные результаты во многом определяются, во-первых, тем, что современный травматолог утрачивает необходимые навыки из-за возможности перейти на другой, для него менее трудоемкий, оперативный метод лечения, а во-вторых, ошибками в выборе показаний к консервативному методу лечения.
Остановимся на показаниях к консервативному методу лечения при изолированных закрытых переломах голени. Я бы их сформулировал следующим образом: стабильные переломы с удавшейся одномоментной или постепенной репозицией; нестабильные переломы с незначительным смещением костных фрагментов. В остальных случаях целесообразно применять оперативное лечение перелома.
В последнее время появляются сообщения о том, что плохо поддаются консервативному лечению внесуставные метадиафизарные переломы в верхней трети голени. А. В. Скоро-глядов с соавт. [1] изучили результаты консервативного лечения таких переломов у 52 больных в нашей клинике и выявили не-сросшиеся переломы у 10 и неправильно сросшиеся переломы у 5 из них. Авторы видят причину таких неблагоприятных исходов
в биомеханических особенностях переломов такой локализации.
Было проведено измерение смещающих сил, воздействующих на костные фрагменты, фиксированные в аппарате Илизарова при помощи пружинных весов. Измерения при нагрузке подтвердили, что при переломах голени на этом уровне возникает прогрессирующее увеличение углового смещения от нижней трети голени по направлению к проксимальному метафизу. Была доказана необходимость создания высокоэффективной защиты этим смещающим усилиям, которая противодействовала бы нарастающему угловому смещению отломков.
А. В. Скороглядов с соавт. считают, что лучшим методом лечения таких переломов является чрескостный остеосинтез с особой расстановкой отдельных элементов аппарата. Очень важным выводом из их работы следует считать, что АНФ следует применять при переломах такой локализации вне зависимости от степени смещения фрагментов, в т. ч. и при переломах без смещения или с хорошей репозицией отломков. Alt et al. [113] анализировали опыт лечения 54 переломов голени в верхней трети и пришли к выводу о том, что это «особые переломы, требующие костной пластики из-за частых нарушений сращения».
По данным Bono et al. [124], внесуставные переломы большеберцовой кости в верхней трети составляют от 5 до 11% переломов ди-афиза голени. Лечение их более сложно, чем переломов, расположенных ниже, гораздо чаще наблюдаются сочетанные повреждения магистральных сосудов, компартмент-синдром. Консервативное лечение во многих случаях заканчивается неправильным сращением (особенно при интактной малоберцовой кости), с выраженной варусной деформацией, поэтому авторы рекомендуют консервативное лечение только при переломах без смещения или с минимальным смещением отломков без серьезных повреждений мягких тканей.
Bono с соавт. считают, что наименее показан при таких переломах остеосинтез пластинками из-за высокого процента инфекционных осложнений и несостоятельности фиксации. В то же время может быть рекомендован комбинированный способ операции: расположение пластинки по наружной поверхности кости в сочетании с наложением стержневого аппарата наружной фиксации по внутренней ее поверхности. Аппаратный метод лечения показан при коротком проксимальном фрагменте и значительном повреждении мягких тканей.
По мнению авторов этой работы, применение интрамедуллярного остеосинтеза может сопровождаться неправильным сращением с вальгусной деформацией голени, и потому этот метод может быть применен только в тех случаях, когда длина проксимального отломка не менее 5-6 см. В этих случаях вход в портал должен располагаться максимально проксимально и кнаружи от связки, а блокирующие винты должны проводиться так, чтобы устранить вальгирование. В заключение авторы пишут, что такие переломы требуют определенного алгоритма действий, который должен определяться тяжестью повреждений мягких тканей, степенью стабильности плоскостей излома и длиной проксимального костного фрагмента.
Оперативное лечение закрытых переломов голени
Все существующие способы остеосинтеза — интрамедуллярный, накостный, аппаратами наружной фиксации и комбинированные способы фиксации — находят свое применение при переломах этой локализации. Хочу коротко вспомнить исторические этапы оперативного лечения переломов голени. Начну с интрамедуллярного остеосинтеза.
Наша клиника, как и вся отечественная травматология, прошла несколько периодов в применении интрамедуллярного остеосинтеза большеберцовой кости: от репозицион-ного, с обязательной дополнительной внешней иммобилизацией гипсовой повязкой, до современного биологического блокирующего остеосинтеза UTN.
Сложная конфигурация костно-мозгового канала и отсутствие сплошной полости [34] этой кости делали невозможным прочную фиксацию перелома на всех уровнях, кроме истмального. Отсутствие возможности операционного рентгенологического контроля в процессе остеосинтеза и применение прямых ригидных стержней в 1960-1970 годы заставляли нас прибегать к открытому ретроградному методу введения стержней. Большинство из ныне читающих эти строки не очень представляют себе такую методику фиксации.
Следующим этапом был открытый прямой остеосинтез стержнями ЦИТО, Охотского-Суваляна, Zimmer и др. Это был уже заметный шаг вперед в сравнении с ретроградным способом. Но и эти способы фиксации обеспечивали стабильность только при переломах на уровне средней трети костной трубки и также часто требовали наложения гипсовой повязки. При переломах в верхней трети часто происходило фиксированное смещение проксимального фрагмента кпереди, а при переломах в нижней и на границе средней и нижней третей большеберцовой кости непреодолимым препятствием оставалась ротационная подвижность дистального костного фрагмента.
Поэтому при переломах в нижней трети голени использовали такие способы остеосинтеза, как фиксацию двумя стержнями Богданова, вводимыми по принципу Раша «вазы с цветами», применяли (без выраженного эффекта) различные способы искусственного сужения канала дистального фрагмента, блокирование плоским титановым стержнем по «ярославской» методике.
В те годы мы считали необходимым добиваться максимально ригидной фиксации перелома и для этой цели применялись максимальные по диаметру стержни, требовавшие рассверливания канала соответственно диаметру имевшихся стержней. Работы В. П. Охотского, А. Г. Суваляна (они были сотрудниками нашей кафедры в то время), казалось бы, подтверждали правильность такого подхода. Уже в конце 1970-х годов в клинике начал применяться и закрытый интрамедуллярный остеосинтез [12, 13]. Показываю результаты такого остеосинтеза стержнем на рис. 4.3.
Наша клиника была одной из первых в стране, которая начала широко применять открытый остеосинтез косых и винтообразных переломов одним или двумя винтами без пластинок. Уже к 1963 г. было выполнено около 150 подобных операций (СО. Португа-лов, О. С. Бродский). Анатомическая репозиция перелома, нейтрализация смещающих усилий винтом и дополнительная иммобилизация высокой гипсовой повязкой обеспечили прямое сращение у подавляющего большинства наших больных.
Перечисленные трудности, при выполнении интрамедуллярного остеосинтеза того времени, обусловили приоритет открытого накостного остеосинтеза при помощи пластинок Лена, Каплана-Антонова, лапчатых пластинок Полякова и др.
Это был уже следующий период развития остеосинтеза диафизарного перелома голени. Он совпал с внедрением в практику технологий AO/ASIF и на долгие годы стал ведущим методом оперативного лечения таких переломов.
Появились новые компрессионные пластинки (DCP), фиксация которыми позволяла исключить необходимость дополнительной иммобилизации перелома. Но с накоплением опыта появлялась и неудовлетворенность исходами таких операций. Выросло число инфекционных осложнений и несросшихся переломов, заметно удлинились сроки консолидации, резко возросло число рефрактур после удаления пластинок, часто фиксировались явления выраженного металлоза и нарушений кровообращения в кортикальном слое под пластинкой.
Сегодня ситуация изменилась кардинально. Эти изменения коснулись как основополагающих концепций биологии кости в условиях перелома, так и принципов внутреннего остеосинтеза. На первый план вышли способы лечения с минимальным повреждением тканей, окружающих кость, отказ от необходимой ранее межфрагментарной компрессии, допустимость (и даже необходимость!) определенной подвижности фрагментов после остеосинтеза, требование соблюдения баланса между стабильностью фиксации и нарушением кровообращения самой кости и мягких тканей вокруг нее.
Надо признать, что некоторые прогрессивно мыслящие специалисты уже много десятилетий назад интуитивно применяли, пусть примитивные, но все же биологические методы фиксации. Прекрасно помню, как в 1959 г. в Мытищинской больнице (я только начинал тогда свою врачебную работу) руководитель хирургического отделения Е. Н. Острогорский произвел открытый остеосинтез перелома шейки плеча с большим смещением отломков, путем создания вколоченного перелома без какой-либо дополнительной фиксации. Наверное, читатель сейчас улыбается, но ведь это было тогда, когда практически оперативный мет
