Переломы у недоношенных
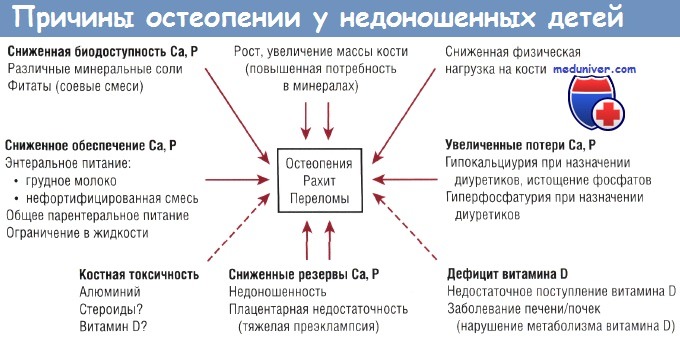
Остеопения и рахит недоношенных новорожденных детей – клиника, диагностика, лечение
Заболевание вызвано сочетанным дефицитом кальция (и фосфора) и витамина D у недоношенных детей. Остеопения недоношенных — это метаболическое заболевание костной ткани, связанное с низкой минерализацией костей скелета. В патогенезе может иметь значение нарушение минерализации зон роста кости, поэтому термины «остеопения недоношенных» и «рахит недоношенных» в литературе часто используют как взаимозаменяемые.
У недоношенных детей после рождения скорость минерализации костей скелета замедлена по сравнению с таковой во внутриутробном периоде, подобно тому как замедляется во внеутробном периоде скорость роста. Наиболее тяжелое осложнение указанной патологии — переломы костей. Чаще всего отмечаются переломы ребер, но переломы длинных трубчатых костей встречаются редко.
Остеопения/рахит отмечается практически у каждого недоношенного ребенка, родившегося с массой тела менее 1500 г. Наиболее тяжелые по состоянию недоношенные дети имеют наиболее выраженную остеопению. Таким образом, частота возникновения рахита (иногда переломов костей) в целом обратно пропорциональна массе тела при рождении. Если тщательно проанализировать результаты рентгенографии, то частота переломов у недоношенных детей колеблется от 20 до 32%. У детей, имеющих массу тела при рождении менее 1000 г, она возрастает до 50-60%.
Описания гистологических изменений при данной патологии немногочисленны. Считается, что ее этиология предполагает участие многих факторов. Как уже было указано ранее, наиболее значимым фактором являются ограниченные запасы кальция (и фосфора) в костной ткани при рождении, а также сниженная скорость минерализации кости по сравнению с внутриутробным периодом.
Остеопения отмечается даже в тех случаях, когда недоношенные дети в качестве питания получают специально разработанные для младенцев с ОНМТ смеси с высоким содержанием минералов или фортификаторы грудного молока.
В опубликованных в последнее время обзорах есть доказательства роли сниженной нагрузки на кость в возникновении остеопении недоношенных. У данной категории младенцев нагрузка на кость ограничена выполнением пассивных или активных мышечных движений. Увеличение нагрузки на кость (например, в виде пассивных движений с вовлечением в работу суставов) способствует формированию костной ткани, в то время как снижение нагрузки (уменьшение физической активности) ведет к резорбции кости.
Две линии доказательств указывают на важность нагрузки на кость у недоношенных детей. Во-первых, было выявлено повышение уровня биохимических маркеров резорбции кости у недоношенных детей (гидроксипролина, телопептида коллагена типа 1, щелочной фосфатазы). Во-вторых, исследования показали, что внедрение программ, стимулирующих пассивную физическую нагрузку у недоношенных детей, улучшает параметры минерализации костной ткани. Удивительно, но программы пассивных упражнений показали свою эффективность, даже если применяли кратковременные упражнения (5-10 мин/сут).
С другой стороны, дефицит витамина D не является частой причиной заболевания костной ткани у недоношенных детей в тех группах, где есть «насыщение» по витамину D. Недоношенные дети с остеопенией обычно имеют нормальные уровни 25(OH)D и повышенные уровни l,25(OH)2D. Пероральный прием витамина D в дозе 2000 ME/ сут в течение 6 нед не влияет на частоту возникновения остеопении у недоношенных детей, что позволяет говорить об адекватности дозы 200-400 МЕ/сут. Другие составляющие патогенеза остеопении недоношенных показаны на рисунке.

Диагноз «остеопения» ставят на основании результатов рентгенологического и лабораторного обследования. Физикальное обследование не столь значимо для выявления заболевания, за исключением тех стадий его развития, когда можно обнаружить крепитацию и припухлость в местах переломов длинных костей. В более старшем возрасте можно выявить рахитические четки в зонах костно-хрящевого соединения и краниотабес.
Поскольку опора на ноги в этом возрасте не столь значима, те очевидные симптомы рахита, которые проявляются искривлением нижних конечностей у детей старшего возраста, не имеют клинического значения.
В большинстве случаев остеопению диагностируют при проведении рутинной рентгенографии, когда выявляют выраженную гипо-минерализацию или признаки произошедших ранее переломов ребер. В случае более тяжелых форм заболевания на стандартных рентгенограммах костей запястья и коленей могут быть видны классические признаки рахита, но обычно они не заметны до двухмесячного возраста ребенка.
Следует указать, что стандартная рентгенография не способна выявить сниженную минерализацию костной ткани до того момента, пока не произойдет потеря 30-40% минерального состава костной ткани. Для проведения в исследовательских целях диагностики костных изменений у недоношенных детей более подходящими считают технологии, обладающие специфической чувствительностью, такие как одиночная фотонная абсорбциометрия, двойная энергетическая рентген-абсорбциометрия, количественная компьютерная томография и трансмиссионная ультразвуковая диагностика.
Для диагностики остеопении недоношенных применяют ряд биохимических маркеров сыворотки крови. Они включают кальций, фосфор, щелочную фосфатазу, паратиреоидный гормон, 25(OH)D, l,25(OH)2D и остеокальцин. Исследуя мочу, можно оценить фракционную экскрецию кальция и тубулярную реабсорбцию фосфата, а также отношение кальций/креатинин. Низкую концентрацию фосфора в сыворотке (менее 45 мг/л) можно считать наилучшим индикатором дефицита минералов у данной категории детей.
Согласно рекомендациям Комитета по питанию Американской академии педиатрии (American Academy of Pediatrics Committee on Nutrition) и некоторых других организаций, в США и Канаде младенцам с ОНМТ, имеющим остеопению, не рекомендуют назначение суточной дозы витамина D более 200-400 ME.
Высокие концентрации l,25(OH)2D и нормальные уровни 25(OH)D практически у всех детей, имеющих указанную патологию, подтверждают правильность упомянутых рекомендаций; детям с ОНМТ не следует назначать в качестве питания продукты, содержащие неадекватное количество кальция и фосфора, например нефортифицированное грудное молоко. Увеличение суточной дозы витамина D до 960 ME и выше не подтвердило эффективности. Потребности в витамине D при парентеральном его введении еще менее ясны.
Впрочем, при использовании современных мультивитаминных препаратов для парентерального введения сложно превысить суточную дозу витамина D 400 ME, не вызывая одновременно передозировки других витаминов-компонентов комплексного препарата. Тем не менее недоношенные дети, длительно получающие полное парентеральное питание, имеют адекватный статус по витамину D даже при получении его в дозе 30-35 МЕ/кг/сут.
Несмотря на то что получены доказательства пользы физической нагрузки (при выполнении пассивных мышечных движений), наиболее важным компонентом профилактики и лечения остается адекватное обеспечение ребенка кальцием и фосфором, без которого любые физические нагрузки на кость будут неэффективными. Вполне логично, что при расчете необходимой дозы минералов преследуют цель достижения скорости минерализации кости, характерной для таковой у плода.
Для этого ребенку необходимо получать энтеральным путем кальций в дозе примерно 200 мг/кг/сут и фосфор в дозе 90 мг/кг/сут, принимая во внимание, что усваивается только 65% кальция (в лучшем случае) и 80% фосфора.
Существуют специальные смеси для детей с ОНМТ, которые позволяют удовлетворить указанные потребности в минералах. Можно также использовать готовые фортификаторы грудного молока, содержащие определенное количество кальция и фосфора. Как уже было сказано ранее, у детей с ОНМТ в первые 8 нед жизни довольно сложно добиться скорости минерализации кости, соответствующей таковой во внутриутробном периоде.
Однако при назначении ребенку кальция и фосфора в указанных ранее дозах можно предотвратить развитие тяжелого рахита и остеопении с переломами костей. Следует отметить, что «наверстывание» минерализации кости будет происходить у этих младенцев еще в течение многих месяцев после выписки из стационара.
Как уже было сказано, профилактика и/или лечение остеопении у детей с ОНМТ, получающих полное парентеральное питание, служит основанием для более пристального внимания к введению некоторых внутривенных растворов. Концентрации кальция и фосфора в них не позволяют достигнуть внутриутробной скорости минерализации кости.
Однако используемые для парентерального питания препараты все же позволяют предупредить переломы костей и развитие рахита. Применение внутривенных препаратов, содержащих 15 ммоль (60 мг/дл) кальция и 15 ммоль (46 мг/дл) фосфора, может способствовать достижению желаемых показателей минерального гомеостаза (как биохимических маркеров, так и уровня кальциотропных гормонов).
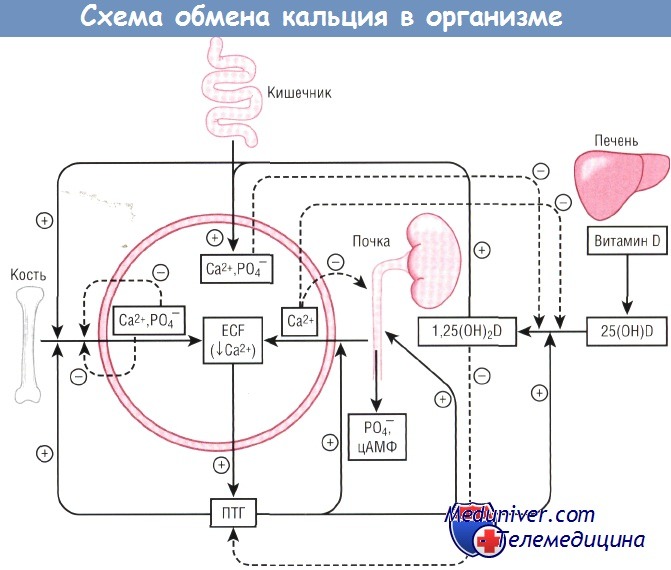
Схема гомеостаза кальция, демонстрирующая взаимодействия между кальцием, кальциотропными гормонами и системой органов.
1,25(OH)2D—1,25-дигидроксивитамин D;
25(OH)D—25-гидроксивитамин D;
ECF — эргокальциферол;
ПТГ — паратиреоидный гормон;
цАМФ — циклический аденозинмонофосфат.
Рахит, обусловленный дефицитом витамина D
В США встречаются случаи рахита у детей ранней возрастной группы, связанные с неадекватным поступлением в организм витамина D и дефицитом солнечного света. Обычно причиной служит выраженный гиповитаминоз D.
Большинство указанных случаев заболевания относились к детям, находящимся исключительно на грудном вскармливании без дополнительного введения витамина D. Следует отметить, что содержание витамина D в грудном молоке минимально. Анализируя случаи рахита у детей, можно отметить, что у этих младенцев часто наблюдалась повышенная пигментация кожи, а также они редко находились под воздействием солнечного света.
Вместе с тем на многих территориях США в зимние месяцы воздействие солнечного света не может считаться достаточно эффективным для синтеза витамина D в коже. Рекомендации по профилактике гиповитаминоза D заключаются в обеспечении всех детей, находящихся на грудном вскармливании, витамином D в дозе 200-400 МЕ/сут до тех пор, пока они не смогут получать адекватное количество витамина D из витамин D-фортифицированных смесей или другой пищи.
– Также рекомендуем “Потребность в витамине А у новорожденных детей”
Оглавление темы “Потребности в витаминах у детей”:
- Потребности в кальции и витамине Д у новорожденных детей
- Ранняя гипокальциемия недоношенных новорожденных детей – клиника, диагностика, лечение
- Остеопения и рахит недоношенных новорожденных детей – клиника, диагностика, лечение
- Потребность в витамине А у новорожденных детей
- Дефицит витамина А и его токсичность у новорожденных детей
- Влияние больших доз витамина А на недоношенных новорожденных детей
- Физиология обмена витамина Е и его эффекты
- Потребность в витамине Е у новорожденных детей
- Дефицит витамина Е у новорожденных детей – клиника, диагностика
- Влияние больших доз витамина Е на недоношенных новорожденных детей
Источник
Цель исследования. Определить частоту и представить клинико-диагностическую характеристику метаболической болезни костей недоношенных (МБКН), протекающей с развитием нетравматических переломов.
Материалы и методы. Исследование проводилось в 2013–2017г.г. Включены все недоношенные дети с переломами на фоне МБКН, не имевшие хирургических заболеваний.
Результаты. Переломы диагностированы у 7 детей: чаще – переломы ребер и бедренной кости, реже – переломы плечевой кости. Все дети получали полное парентеральное питание – от 9 до 43 (медиана 19) суток; у 5 – энтеральное питание не обеспечивало их физиологических потребностей. У всех наблюдалась выраженная гипофосфатемия на 1-м месяце жизни, уровень щелочной фосфатазы повышался у 5 пациентов.
Заключение. Переломы костей вследствие МБКН наблюдались у 2,1% детей с массой тела при рождении менее 1500г (6,25% – с ЭНМТ; 0,4% – с ОНМТ). Все дети имели сочетанные факторы риска развития МБКН. У 3 детей была поздняя диагностика на фоне консолидации перелома кости.
Совершенствование реанимации и интенсивной терапии глубоконедоношенных новорожденных привело к повышению выживаемости детей с очень низкой массой тела (ОНМТ) и экстремально низкой массой тела (ЭНМТ) при рождении, что повлекло за собой появление новых вопросов, связанных с дальнейшим выхаживанием этих пациентов, а также с диагностикой и терапией особых состояний и заболеваний, встречающихся у данного контингента детей. Одним из таких заболеваний, которое осложняет состояние и развитие глубоконедоношенного ребенка, является метаболическая болезнь костей или остеопения недоношенных [1–4].
Метаболическая болезнь костей недоношенных (МБКН) характеризуется изменениями костей вследствие недостатка минеральных веществ, главным образом кальция и фосфора, и/или витамина D, ассоциированных с недоношенностью [3, 5].
Остеопения развивается у 23–30% детей с ОНМТ и у 31–55% детей с ЭНМТ, при этом частота переломов костей у недоношенных с ЭНМТ может достигать 7–10%, однако, предполагается, что частота остеопении в последние годы снижается [6–8].
До настоящего времени диагностика МБКН продолжает основываться, в основном, на рентгенологических данных. Однако наличие лучевой нагрузки и отсутствие унифицированных рентгенологических критериев остеопении недоношенных затрудняет широкое применение данного метода [1, 4–6, 9]. Ограничение использования рентгенологического метода у недоношенных детей в совокупности с неспецифической клинической картиной и отсутствием четких биохимических маркеров МБКН затрудняет верификацию диагноза.
Цель исследования: определить частоту и представить клинико-диагностическую характеристику МБКН, протекающей с развитием нетравматических переломов.
Материал и методы
Исследование проведено на базе отделений ФГБУ «Национального медицинского исследовательского центра акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» МЗ РФ в период с января 2013г. по декабрь 2017г. В исследование вошли все недоношенные дети, у которых на фоне МБКН были диагностированы нетравматические переломы. Критерии исключения: дети с синдромальной и наследственной патологией, а также с хирургическими заболеваниями.
В работе учитывались: гестационный возраст (ГВ), масса тела и рост ребенка при рождении, соответствие массы и роста новорожденного гестационному возрасту (по Fenton preterm grows chart, 2013), пол; анализировались данные по питанию (длительность полного парентерального питания, возраст достижения полного энтерального питания, соответствие питания физиологическим потребностям недоношенного), наличие некротизирующего энтероколита нехирургических стадий (НЭК), бронхолегочной дисплазии средне-тяжелой и тяжелой степени (БЛД) и синдрома холестаза.
При физикальном осмотре регистрировались клинические признаки МБКН: деформация черепа («башенный» череп, «олимпийский» лоб, уплощение черепа с боков, краниотабес), деформация грудной клетки с образованием Гаррисоновой борозды, относительно короткие конечности, задержка роста.
Диагностика переломов основывалась на рентгенологических методах исследования костей (рентгенография, мультиспиральная компьютерная томография (МСКТ)). Рентгенологические признаки остеопении характеризовались в соответствии с классификацией Koo W.W. et al. (1982–1984): потеря плотности белой линии метафиза и истончение кортекса – «стадия 1», «чашевидные» просветленные метафизы и субпериостальные разрастания – «стадия 2»; переломы на этом фоне – «стадия 3» [4, 5, 10].
Ретроспективно оценивались результаты определения в сыворотке крови уровней общего кальция, фосфора, щелочной фосфатазы (биохимический анализ крови), а также концентрации витамина D (иммуноферментный метод).
Проведен анализ медикаментозной терапии, которая негативно влияет на фосфорно-кальциевый обмен: применение кофеина, фуросемида, дексаметазона, фенобарбитала.
Результаты исследования
За 5 лет наблюдения (201…
- Rustico S.E., Calabria A.C., Garber S.J. Metabolic bone disease of prematurity. J. Clin. Transl. Endocrinol. 2014; 1(3): 85-91.
- Chin L.K., Doan J., Teoh Y.S., Stewart A., Forrest P., Simm P.J. Outcomes of standardised approach to metabolic bone disease of prematurity. J. Paediatr. Child Health. 2018; 54(6): 665-70.
- Nallagonda S., Nallagonda M., Deorukhkar A. Metabolic bone disease of prematurity – an overview. Paediatr. Child. Health. 2017; 27(1): 14-7.
- Moreira A., Jacob R., Lavender L., Escaname E. Metabolic bone disease of prematurity. NeoReviews. 2015; 16( 11): e631-41.
- Patole S., ed. Nutrition for the preterm neonate. A clinical perspective. Springer; 2013.
- Viswanathan S., Khasawneh W., McNelis K., Dykstra C., Amstadt R., Super M. et al. Metabolic bone disease: a continued challenge in extremely low birth weight infants. JPEN J. Parenter. Enteral Nutr. 2013; 38(8): 982-90.
- Smurthwaite D., Wright N.B., Russell S., Emmerson A.J., Mughal M.Z. How common are rib fractures in extremely low birth weight preterm infants? Arch. Dis. Child. Fetal Neonatal Ed. 2009; 94(2): F138-9.
- Gomella T.L., Cunningham M.D., Eyal F.G., eds. Neonatology: management, procedures, on-call problems, diseases, and drugs. 7th ed. McGraw-Hill; 2013.
- Нароган М.В., Рюмина И.И., Степанов А.В. Остеопения (метаболическая болезнь костей) у недоношенных: возможности диагностики, лечения и профилактики. Неонатология. 2014; 3: 77-83.
- Koo W.W., Gupta J.M., Nayanar V.V., Wilkinson M., Posen S. Skeletal changes in preterm infants. Arch. Dis. Child. 1982; 57(6): 447-52.
- Ukarapong S., Venkatarayappa S.K.B., Navarrete C., Berkovitz G. Risk factors of metabolic bone disease of prematurity. Early Hum. Dev. 2017; 112: 29-34.
- Machado A., Rocha G., Silva A.I., Alegrete N., Guimarães H. Bone fractures in a neonatal intensive care unit. Acta Med. Port. 2015; 28(2): 204-8.
- Dabezies J., Warren P.D. Fractures in very low birth weight infants with rickets. Clin. Orthop. Relat. Res. 1997; (335): 233-9.
- Lyon A.J., McIntosh N., Wheeler K., Williams J.E. Radiological rickets in extremely low birthweight infants. Pediatr. Radiol. 1987; 17(1): 56-8.
- Ионов О.В., Балашова Е.Н., Ленюшкина А.А., Киртбая А.Р., Кухарцева М.В., Зубков В.В. Сравнение двух стартовых схем – быстрого и медленного увеличения объема энтерального питания у новорожденных с очень низкой массой тела в условиях отделения реанимации и интенсивной терапии. Неонатология: новости, мнения, обучение. 2015; 4: 73-81.
- Грошева Е.В., Ионов О.В., Ленюшкина А.А., Нароган М.В., Рюмина И.И. Энтеральное вскармливание недоношенных детей. В кн.: Иванов Д.О., ред. Клинические рекомендации (протоколы) по неонатологии. СПб.: Информ-Навигатор; 2016: 252-70.
- Montaner R.A., Fernández E.C., Calmarza C.P., Rite G.S., Oliván Del Cacho M.J. Risk factors and biochemical markers in metabolic bone disease of premature newborns. Rev. Chil. Pediatr. 2017; 88(4): 487-94.
- Gaio P., Verlato G., Daverio M., Cavicchiolo M.E., Nardo D., Pasinato A. et al. Incidence of metabolic bone disease in preterm infants of birth weight
- Tinnion R.J., Embleton N.D. How to use… alkaline phosphatase in neonatology. Arch. Dis. Child. Educ. Pract. Ed. 2012; 97(4): 157-63.
- Ali E., Rockman-Greenberg C., Moffatt M., Narvey M., Reed M., Jiang D. Caffeine is a risk factor for osteopenia of prematurity in preterm infants: a cohort study BMC Pediatr. 2018 18(1) 9.
Поступила 15.06.2018
Принята в печать 22.06.2018
Кухарцева Марина Вячеславовна, врач неонатолог отделения патологии новорожденных и недоношенных детей ФГБУ НМИЦ АГП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4.; аспирант кафедры Неонатологии, ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет). 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2. E-mail: m_kukhartseva@oparina4.ru
Нароган Марина Викторовна, д.м.н., в.н.с. отделения патологии новорожденных и недоношенных детей ФГБУ НМИЦ АГП им. академика В.И. Кулакова
Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4.; профессор кафедры неонатологии, ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2. E-mail: m_narogan@oparina4.ru
Козлова Алина Владимировна, врач рентгенолог отделения лучевой диагностики ФГБУ НМИЦ АГП им. академика В.И. Кулакова Минздрава России.
Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. E-mail: av_kozlova@oparina4.ru.
Рюмина Ирина Ивановна, д.м.н., руководитель отделения патологии новорожденных и недоношенных детей ФГБУ НМИЦ АГП им. академика В.И. Кулакова
Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. Телефон: 8 (903) 770-80-48. E-mail: i_ryumina@oparina4.ru
Орловская Ирина Владимировна, к.м.н., заведующая по клинической работе отделения патологии новорожденных и недоношенных детей ФГБУ НМИЦ АГП
им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. E-mail: i_orlovskaya@oparina4.ru
Парнас Александра Юрьевна, студентка 5 курса педиатрического факультета, РНИМУ им. Н.И. Пирогова. Адрес: 117997, Россия, Москва, ул. Островитянова, 1.
Семенова Ольга Евгеньевна, студентка 5 курса лечебного факультета, ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет). 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2.
Зубков Виктор Васильевич, д.м.н., профессор, заведующий отделом неонатологии и педиатрии ФГБУ НМИЦ АГП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4.; профессор кафедры неонатологии, ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2. E-mail: v_zubkov@oparina4.ru
Дегтярев Дмитрий Николаевич, д.м.н., профессор, заместитель директора по научной работе ФГБУ НМИЦ АГП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4., заведующий кафедры неонатологии, ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2. E-mail: d_degtiarev@oparina4.ru
Для цитирования: Кухарцева М.В., Нароган М.В., Козлова А.В., Рюмина И.И., Орловская И.В., Парнас А.Ю., Семенова О.Е., Зубков В.В., Дегтярев Д.Н. Клинико-диагностические аспекты нетравматических переломов при метаболической болезни костей недоношенных. Акушерство и гинекология. 2019; 3: 106-13.
https://dx.doi.org/10.18565/aig.2019.3.106-113
Источник
